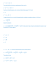tarea2-soluciones
Transcripción
tarea2-soluciones
Soluciones a la Tarea 2. Física Estadística March 3, 2015 1. El calor especíco molar a volumen constante de un gas ideal monoatómico es 32 R. Suponer que un mol de este gas es sometido a un proceso cíclico y cuasiestático siguiendo una trayectoria circular en el diagrama P V . Encontrar las siguientes cantidades: a) b) c) El trabajo neto (en Joules) realizado por el gas en un ciclo. La diferencia en la energía interna del gas entre el estado C y el A. El calor absorbido por el gas al ir del punto A al C a través de la trayectoria ABC del ciclo. Figure 1: Trayectoria circular en el diagrama PV Solución: (a) Tenemos que el trabajo está dado por el área encerrada por la curva que sigue la trayectoria circular del punto A→C menos el área encerrada al ir del punto C → A, lo que da como resultado que el trabajo es igual al área que encierra la circunferencia, multiplicado por las respectivas unidades de volumen y presión Z Wtotal = C Z A p dV − A C 1dyn = 10−5 N. dyn p dV = π(1)3 106 2 (103 cm3 ) = 3.14102 J = 314J cm 1 (1) (b) La energía para un gas ideal es sólo función de la temperatura además de satisfacer nRT y ser monoatómico con una capacidad caloríca de cv = 3/5R, PV = por lo que el cambio en la energía interna está dado por, 3 3 3 ∆E = cv ∆T = (P C V C − P A V A ) = P A (V C − V A ) = × (4 × 102 )J = 600J 2 2 2 (2) (c) Antes que nada debemos calculare el area encerrada por la trayectoria al ir del punto A → C, por la curva ABC , esta área es igual al área del semicírculo más el área del cuadrado que está debajo del semicírculo: Z Wtotal = C pdV = A 314 J + 400J = 157J + 400J = 557J 2 (3) A partir del trabajo podemos calcular el calor absorbido durante el proceso aplicando la segunda ley de la termodinámica, Q = ∆E + W = 557J + 600J = 1157J 2. (4) A continuación se describe el método usado para medir la razón de calores especícos γ ≡ Cp /Cv de un gas. Un gas, el cual se supone ideal, se conna dentro de un contenedor cilíndrico vertical que posee un pistón de masa m que se puede mover libremente. Tanto el pistón como el cilíndro tienen la misma sección transversal de área A. La presión atmosférica es p0 , cuando las fuerzas debido a la gravedad están en equilibrio con la debida a la presión del gas en el cilíndro, el volumen del gas es V0 . Suponga que el pistón es desplazado levemente de su posición de equilibrio, oscilando sobre esta posición con frecuencia ν . Considera que las oscilaciones son sucientemente lentas, de tal forma que el gas permanece en equilibrio interno, pero sucientemente rápidas para permitir que el gas no experimente un intercambio de calor con los alrededores. Por lo que las variaciones en la presión del gas como en el volumen son adiabáticas. Expresa γ en términos de de m, g , A, p0 , V0 y ν . Solución: Sea p la presión ejercida por el gas y V el volumen debajo del pistón. El gas sufre un cambio cuasi-estático y adiabático de tal manera que durante las oscilaciones del pistón, la relación, pV γ = cte, (5) [p(0) + δp][V0 + δV ]γ = p(0)V0γ , (6) De aquí podemos escribir, δV [p(0) + δp] 1 + V0 γ = p(0) (7) Las oscilaciones alrededor del equilibrio mecánico son pequeñas, así que en cualquier instante dado durante la oscilación se satisface, δV V0 2 y δp p(0), por lo tanto, " #! δV γ δV 2 δV [p(0) + δp] 1 + +O = [p(0) + δp] 1 + γ V0 V0 V0 " # δV 2 δV +O = p(0) = p(0) + δp + γp(0) V0 V0 Por lo tanto, V0 δp V0 δ(pA) =− p(0) δV p(0)A δ(Ay) V0 δF =− 2 (mgA + p0 A ) δy γ=− donde F es la fuerza ejercida por el gas sobre el pistón a cualquier instante de tiempo durante la oscilación, de tal forma que δF = F − F (0) y δy es el desplazamiento desde la posición de equilibrio en ese instante. Considerando que el pistón ejecuta un movimiento armónico simple (no hay amortiguamiento ya que el gas no intercambia calor durante las oscilaciones), tenemos, Fpistón = F − p0 A − mg = −kδy = −ω 2 mδy. (8) δF = (−ω 2 mδy + p0 A + mg) − (p0 A + mg) = −ω 2 mδy. (9) Entonces, Usando ω = 2πν , para la frecuencia angular, obtenemos, γ= 3. ω 2 mV0 4π 2 ν 2 mV0 = mgA + p0 A2 mgA + p0 A2 (10) Cuando una onda de sonido atraviesa a un uido (líquido o gas), el período de vibración es pequeño comparado con el tiempo de ralajación necesario para que un elemento de volumen de tamaño macroscópico del uido intercambie energía con el resto del uido por medio del ujo de calor. Por lo tanto las compresiones de un elemento de volumen pueden ser consideradas adiabáticas. Analizando las compresiones unidimensionales y los enrarecimientos del uido en un bloque de espesor dx, muestre que la presión p(x, t) en el uido depende de la posición x y el tiempo t de tal manera que satisface la ecuación de onda. 2 ∂2p 2∂ p = u ∂t2 ∂x2 (11) 1 Donde la velocidad de propagación de sonido u es una constante dada por u = (ρκs )− 2 . Aquí ρ es la densidad de equilibrio del uido y κs es la compresibilidad adiabática dada por κs = −V −1 ( ∂V ∂p )s . Solución: 3 Cuando el sonido atraviesa un uido, i. e., un gas o líquido, el desplazamiento es a lo largo de la dirección longitudinal porque los uidos transmiten pobremente las fuerzas corte ( shear) necesarias para mantener una onda transversa. Los lugares donde las moléculas del uido se agrupan se llaman condensaciones y donde las moléculas se separan rarefacciones. Las leyes de los gases sugieren que las regiones de alta densidad de un uido gaseoso están a más alta presión (fuerza por unidad de area) y las regiones de baja densidad a menor presión. Para obtener la ecuación de onda unidimensional, jemonos en un elemento pequeño de volumen del uido. Este elemento de volumen efectúa un movimiento armónico, cuando el sonido se transmite. Si aplicamos un gradiente de presión al elemento vi (como la presión acústica de una onda de sonido), se moverá y comprimirá el volumen del uido. La presión en la cara izquierda del bloque es presión diferencial p1 (x1 ), mientras que la que se ejerce a la derecha es p2 (x2 ). Si hay una ∆p, entonces el bloque de uido se moverá a la derecha y mientras el bloque vf . Supondremos que el proceso es adibático, es decir, no se acelera, cambiará su volumen a gana o pierde calor debido a la transmisión de la onda de sonido y además que los cambios en los desplazamientos de las partículas del uido, desde sus puntos de equilibrio, son pequeños. Además, supondremos que la columna del uido no se deforma (deformación de corte) debido a la presión diferencial. Para describir el movimiento de la onda en el uido, partimos de la segunda ley de Newton y la conservación de la masa. Las fuerzas a lo largo de la dirección volumen vi x, sobre el elemento de son, p(x1 )A − p(x2 )A = −∆pA (12) La fuerza neta a través del elemento es igual a la masa por la aceleración del volumen. La masa está dada por m = ρ1 A∆x. La aceleración en la dirección x es la segunda derivada del desplazamiento promedio, ax = donde s = (s1 + s2 )/2. ∂2s ∂t2 (13) Por lo tanto, − ∆pA = ρ1 A∆x ∆p − = ρ1 ∆x ∂2s ∂t2 ∂2s ∂t2 (14) (15) considerando la presión acústica (ya que la derivada de la presión estática es cero) y la densidad ρ para un elemento de volumen innitesimal, obtenemos, ∂pa = −ρ ∂x ∂2s ∂t2 (16) El módulo de compresibilidad adiabática, describe que tanto cambia el volumen del uido debido a un cambio en la presión, 4 1 p(x1 ) − p(x1 ) pa ≡− ≈− . κs (vf − vi )/vi ∆v/vi El signo negativo indica que cuando pa es positivo, vf < v1 y ∆v (17) es negativo. Podemos obtener geométricamente una expresión que relaciona a la presión acústica con el desplazamiento del elemento de volumen (ley de conservación de la masa). Suponiendo que no hay fuentes ni sumideros en el elemento de volumen, vi = A∆x vf = A(∆x + ∆s) (vf − vi ) ∆s ∆v A(∆x + ∆s) − A∆x = . = = vi vi A∆x ∆x (18) Sustituyendo la ecuación 18 en 17, pa = − 1 ∆s 1 ∂s ≈− . κs ∆x κs ∂x Por lo tanto, 1 ∂2s ∂pa =− . ∂x κs ∂x2 (19) Sustituyendo la ecuación 19 en la ecuación 16 obtenemos la ecuación de onda unidimensional, ∂2s ∂2s = ρκ , s ∂x2 ∂t2 que describe el desplazamiento s (20) desde la posición de resposo de las partículas en un medio, con respecto al tiempo y la posición. 4. Muestra que la energía libre de Helmholtz F (T, V, N ) de un sistema con volumen V en contacto con un baño caloríco a temperatura T es un mínimo en equilibrio. De igual manera, muestra que la energía libre de Gibbs G(T, P, N ) de un sistema en contacto con un baño a temperatura T y presión P es un mínimo en equilibrio. Solución: Partiendo de que no se puede asignar una temperatura denida a un sistema con volumen y en contacto con un baño caloríco a la temperatura entonces la energía libre de Helmholtz F T V jo si ambos no están en equilibrio térmico, no es una función bien denida de la temperatura y volumen. Sin embargo, podríamos denir una energía libre de acuerdo a la relación, F = U − T S, donde se entiende que U es la energía interna del sistema, la cual esta bien denida aún cuando el sistema no este en equilibrio y T la temperatura del baño caloríco, la cual es la misma 5 temperatura del sistema una vez que alcance el equilibrio. La entropía de no equilibrio S del sistema no es simplemente una función de U y V, sino que depende de los detalles del estado de no equilibrio. Usando el principio de Clausius de la segunda ley, δS ≥ con δQ T (21) δQ una porción de calor transferido desde el baño caloríco al sistema. Ya que el volumen del sistema es constante y no se efectúa trabajo cuando se transere este calor, el cambio en la energía interna del sistema es δU = δQ. Como la temperatura T del baño caloríco esta ja, obtenemos, δF = δU − T δS = δQ − T δS ≤ 0. Es decir, F siempre decrece cuando el sistema se aproxima al equilibrio y alcanza un mínimo cuando llega al mismo. Por otro lado, para la energía libre de Gibbs sistema cuya presión al equilibrio. P G = U + P V − T S, debemos considerar un se mantiene ja, pero cuyo volumen es variable cuando se aproxima Aquí los cambios en energía estan dados por la expresión δU = δQ − P δV y siguiendo un argumento similar al previo obtenemos, δG = δU + P δV − T δS = δQ − T δS ≤ 0. Nótese que F es útil para describir un sistema cuya temperatura y volumen están controla- dos externamente, mientras que G es de utilidad cuando la temperatura y la presión están controladas externamente. 5. Explique lo que ocurre en la transición isotrópico-nemático de un cristal líquido. Solución: Para sistemas compuestos de moléculas que son anisotrópicas (generalmente con forma de barras o hebras rígidas) pueden inducir una anisotropía macroscópica, es decir, una fase nemática. A densidades sucientemente bajas, las barras pueden tener suciente libertad para acomodarse y orientarse, esto hará que el uido sea isotrópico. Sin embargo, conforme la densidad aumenta, es más difícil que las barras apunten en direcciones aleatorias, por lo tanto, comienza a ser más signicativa la correlación de la orientación de las barras. De esta manera es que se forma un eje privilegiado en el sistema. Intuitivamente uno podría esperar que en algún punto hay una transición de fase. 6. Muestre que una sustancia cuya curva de fusión tiene una pendiente negativa, tal como el hielo o el bismuto, se contrae al derretirse (Hint: Ecuación de Clapeyron). Solución: Partiendo de la ecuacíon de Clapeyron: dp ` T ∆s ∆s = = = dT T ∆v T ∆v ∆v 6 (22) Si la pendiente es negativa tenemos ∆s/∆v < 0. En el proceso de fusión hay un cambio de sólido a líquido por lo que, Por lo tanto, ∆v < 0, s` > ss → ∆s > 0 (23) v` < vs , (24) esto es, entonces la sustancia se contrae. 7