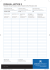
Soluciones y Concentraciones
Transcripción
Soluciones y Concentraciones
CPU CPU Soluciones Calle Mercado # 555 Calle Mercado # 555 Teléfono 3 - 366191 Sal (Soluto) Definición de Concentración Solución Diluida Solución Concentrada Salmuera (Solución) poco soluto Concentración Unidades Químicas Porcentual en peso (masa/masa) Concentración Molar (Molaridad) masa soluto masa solucion 100% M= mol soluto litros solucion N= #Eq soluto litros solucion Porcentaje en volumen (volumen/volumen) P % (V/V) = Volumen soluto Volumen solucion 100% Porcentaje masa - volumen P % (m/V) = gramos soluto ml solucion 100% C (m/V) = Partes por millón ppm = ppm = gr soluto solucionPeso Molecular gr soluto litros solucionPeso Equivalente Concentración molal (molalidad) Molar y Normal N = nM mol soluto kg solvente n= ò ó valencia del metal ò subindice del metal mg soluto kg solucion X solvente = mol solvente mol soluto +mol solvente Dilución Agregando solvente Agregando Soluto C 1V 1 = C 2V 2 m 1P 1 = m 2P 2 M 1V1 + n = M 2V2 Mezclando dos soluciones C 1 V 1 + C 2V 2 = C 3 V 3 V 1D 1P 1 + V 2D 2P 2 = V 3D 3P 3 V1 + V2 = V3 m 1P 1 + m 2P 2 = m 3P 3 m1 + m2 = m3 Vi = Volumen de Solución mi = Masa de solución Pi = Porcentaje en peso C 1( m/V )V 1 + m soluto = C2 (m/V) V 2 m 1 P 1 + m soluto 100% = m 2P 2 V 1D 1 P 1 = V 2 D 2 P 2 N 1V 1 + #Eq = N 2V2 V1 D 2P 1 + m soluto 100% = V2 D 2 P 2 M = Concentración Molar N = Concentración Normal C(m/V) = Concentración masa -volumen Ci = Concentración Molar, Normal o masa - volumen n = Número de moles de soluto #Eq = Número de equivalentes químicos de soluto msoluto = Masa de soluto Di = Densidad de Solución Descenso Crioscópico P Vsolucion = P V solventeX solvente T e = K e m T c = K c m T e = Te solucion Te solvente puro T c = T c solvente puro T c solucion ∆Τe = Aumento Ebulloscópico (ºC) nRT V ∆Tc = Descenso Crioscópico (ºC) Ke = Constante Ebulloscópica (de ebullición) Kc = Constante Crioscópica (de congelación) π = Presión Osmótica n = Número de moles T = Temperatura (ºK) V = Volumen R = 62, 36 mmHgl Kmol Te = Temperatura de ebullición (ºC) Tc = Temperatura de congelación (ºC) m = Concentración molal Termometría Crioscópicas Ebulloscópicas K273 C Kc Te Tc Ke = 5 = F32 = R a492 = R4e 5 9 9 Acido acético 16,6ºC 3,90 111,1ºC 3,07 0,0ºC 1,86 100ºC 0,52 K = C + 273 F = 9C + 32 C = 5(F32) Agua 5 9 5,48ºC 5,10 80,08ºC 2,57 F = Ra 460 Benceno R a = Rankine Cloroformo -63,5ºC 4,67 61,3ºC 3,86 C = Celsius o Centigrado R e = Reamur K = Kelvin CCl 4 ------- ------- 76,8ºC 5,05 F = Farenheit Unidades de Conversión Constantes ó Fracción Molar mol soluto X soluto = molsoluto +mol solvente masa soluto Volumen solucion mg soluto litro solucion N= Aumento Ebulloscópico = Concentración Normal (Normalidad) m= Concentración masa - volumen M = litros Ley de Raoult Pv = Presión de vapor X = Fracción Molar Presión Osmótica mucho soluto Concentración Unidades Físicas P % (m/m) = Las Soluciones Teléfono 3 - 366191 Definición de Solución Agua (Solvente) Propiedades de Solventes Presión Bar 100 kPa 10 milibar 100 Pa 10 Baria 1cm Hg = 10 mm Hg Kl 10 1000 Hl Hm 10 1000 Dl Dm3 Dg 10 1000 l m3 g dg cl cg dm3 10 1000 ml mg mm3 1 lb / plg = 51,71 Torr 1 pie (ft) = 0,3048 m 1 plg (in) = 0,0254 m 1 cm = 1ml 1Tm = 1000 kg 1 pie (ft) = 12 plg (in) 1 utm = 9,8 kg 1 slug = 14,59 kg 1 lb = 0,4536 Kg = 453,6 g M = Metal n= ò ó ò ó valencia subindice del metal del metal Hidróxido 1EqM(OH) n = Peso Molecular nro de OH (n) Sal 1 atm = 760 Torr 2 3 3 X = No metal 3 cm 10 1000 1 pie3 = 0,0283168 m3 Peso Equivalente o Equivalente Químico Símbolos Valor de "n" 10 1000 dl 1 m3 = 1Kl 1 dm = 1l 3 Hg 1 mm Hg = 1 Torr 1 Bar = 750 mm Hg Km3 Kg 1Eq ( H nXO) = Peso Molecular nro de H + (n) Óxidos y Anhídridos 2 1mm Hg = 13,6 kp/m 1 atm = 101325 Pa = 760 mmHg Acido 1Eq (MXO) = Peso Molecular n 1Eq (MO) = Peso Molecular n