Diagnóstico - Revista Panamericana de Infectología
Transcripción
Diagnóstico - Revista Panamericana de Infectología
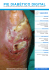
Lima ALLM, et al. • Directrices panamericanas para el tratamiento de las osteomielitis... CAPÍTULO II Diagnóstico Este capítulo aborda la importancia de los exámenes para la confirmación diagnóstica de las osteomielitis. Ponemos de relieve: evaluación del cuadro clínico del paciente, confirmación de sospechas por medio de exámenes laboratoriales, exámenes anatomopatológicos, exámenes microbiológicos. Igualmente se discute los avances en el diagnóstico microbiológico de las osteomielitis, las recomendaciones para recolección, transporte y procesamiento de muestras, la aplicación de imagen en los avances diagnósticos, y la medicina nuclear con el centellograma óseo Diagnóstico clínico En adultos, las osteomielitis son generalmente secundarias a fracturas expuestas, a las cirugías ortopédicas con o sin colocación de implantes o relacionadas a la presencia de diabetes melittus e insuficiencia vascular periférica.(1) El diagnóstico adecuado de las infecciones óseas enfrenta muchas dificultades, pues la estandarización de los métodos de investigación diagnóstica no es ampliamente aceptada, y las señales y síntomas clínicos en conjunto con los testes de actividad inflamatoria son inespecíficos. Los exámenes de imagen pueden ser poco aclaradores en la fase aguda de la enfermedad o poco específicos en la fase crónica y la obtención de tejido óseo para las culturas, a pesar de definitivo, no siempre contribuyen para el diagnóstico. De este modo, el diagnóstico de osteomielitis requiere un conjunto de señales y síntomas clínicos, testes laboratoriales, exámenes de imagen, análisis histopatológica y finalmente la identificación de lo(s) patógeno(s) por medio de las culturas del tejido óseo o de hemoculturas, principalmente en los casos de osteomielitis hematógena. La variabilidad de los hallazgos diagnósticos está asociada a la duración y sitio de infección, extensión de la inflamación, presencia de implantes.(1) Cuadro clínico La sospecha clínica es fundamental para la investigación de la enfermedad, y sus manifestaciones clínicas dependen de varios factores como: tipo (aguda o crónica) y local de la infección y tipo de hueso implicado.(1,2) En las formas agudas de osteomielitis y en las de origen hematógena, los síntomas locales como dolor, calor, edema e hiperemia y los síntomas sistémicos como fiebre, mal estar general y adinamia aparecen hasta dos semanas después de la infección. Sin embargo, la presentación clínica de las osteomielitis puede ser significativamente variable, y es fácil la sospecha diagnóstica en pacientes que presentan fístula cutánea o herida abierta con exposición ósea seguida de fractura expuesta; y muy difícil en los pacientes que presentan tan solo dolor progresivo.(2) En las formas crónicas de osteomielitis la presentación clínica es muy variable, los síntomas sistémicos están generalmente ausentes y los síntomas locales como hiperemia, calor, tumoración y fistulización aparecen muchas veces de forma intermitente o incluso años después del comienzo de la infección ósea.(2) En algunos casos, puede haber limitación de movimiento cuando hay destrucción ósea, participación articular o del disco intervertebral.(1) 17 Rev Panam Infectol 2013;15(1 Supl 1):17-25. En los pacientes portadores de diabetes, señales inflamatorios discretos de piel y tejidos blandos (celulitis) o úlceras en áreas de prominencia ósea sin señales o síntomas sistémicos pueden ser sugestivos de osteomielitis. En las úlceras de pie diabético la presencia de exposición ósea o del teste de palpación del pie con instrumento de metal de punta contundente a través de la ulceración presenta sensibilidad y especificidad de 60% y 90%, respectivamente.(3) Diagnóstico laboratorial inespecífico Exámenes laboratoriales En el hemograma, leucocitosis con neutrofilia está generalmente presente en las infecciones agudas y raramente en las osteomielitis crónicas. Testes de actividad inflamatoria como velocidad de hemosedimentación (VHS) y dosis de proteína-C reactiva (PCR) están frecuentemente más elevados en las osteomielitis agudas hematógenas en niños, pero, son testes inespecíficos y son de más ayuda para el control de tiempo de antibióticoterapia.(4,5) Niveles poco elevados de PCR y VHS en pacientes con antecedentes de manipulación quirúrgico y dolor crónico y persistente puede ayudar en la sospecha de la enfermedad e inducir el médico a progresar en la investigación diagnóstica adecuada. La dosis de procalcitonina sérica para el diagnóstico o seguimiento de osteomielitis hematógena en niños o en diabéticos no ha mostrado ser eficiente en pocas series de casos.(6-8) La dosis sérica de interleucina-6 es más estudiada como herramienta diagnóstica de las infecciones óseas asociadas a las prótesis articulares.(9) Exámenes anátomo-patológicos Muestras de hueso, tejidos blandos y del secuestro óseo deben ser conducidas para análisis histopatológica luego de la biopsia ósea y pueden confirmar el diagnóstico de osteomielitis con la observación de necrosis ósea, con extensa reabsorción y exudado inflamatorio.(2,10,11) En las osteomielitis agudas predominan los leucocitos polimorfonucleares y en las formas crónicas predominan los linfocitos, osteoblastos y osteoclastos. En las infecciones asociadas a la osteosíntesis, la reacción inflamatoria es predominantemente medular.(10) En la sospecha de osteomielitis, el examen histopatológico fue responsable por la confirmación diagnóstica en 50% de los pacientes.(12) Muestras congeladas de tejido óseo obtenidas en el intraoperatorio con más de cinco neutrófilos por campo presentan sensibilidad que cambia de 43% a 84% y especificidad de 93% a 97% en las infecciones óseas asociadas a los implantes ortopédicos.(2,13) La 18 presencia de lesiones granulomatosas con la coloración de Ziehl-Neelson positiva caracteriza infección por Micobacteria.(2) Diagnóstico laboratorial específico Exámenes microbiológicos El diagnóstico de certidumbre de osteomielitis es realizado con la identificación microbiológica del patógeno en el hueso por medio de biopsia ósea.(11,12) Teniendo en cuenta que el tiempo de tratamiento antibiótico en las osteomielitis es prolongado y que por lo menos la mitad de las infecciones puede ser causada por bacterias Gram negativas con perfil de sensibilidad variable para cada servicio, y que muchas infecciones son igualmente causadas por Staphylococcus aureus multiresistente (MRSA) y productores de biofilm, recolectar muestras de tejido óseo para cultura es fundamental para el manejo adecuado de esta enfermedad. Materiales obtenidos por medio de swabs de fístula o de secreciones para cultura resultará en falso positivos, ya que identifica microorganismos que colonizan la piel. Además de eso, estudios en pacientes con osteomielitis crónica y en los diabéticos demuestran que partes quitadas de tejidos blandos para cultura detectan bacterias diferentes de las culturas quitadas del hueso y la similitud de identificación de bacterias entre estas distintas fuentes de recolección puede llegar a menos de 50%.(14) La cultura de tejido óseo que se obtiene durante procedimiento quirúrgico, o por medio de punción percutánea, puede ser positiva en 60 a 80% de los casos y culturas del secuestro óseo pueden identificar los patógenos en hasta 87% de los casos de osteomielitis.(10,11) Preferentemente, se debe producir por lo menos tres muestras diferentes de tejido óseo, y con el objetivo de aumentar la positividad del teste, las culturas deben ser producidas con antelación al comienzo de la antibioticoterapia.(11,12) Bacterias de crecimiento lento como Propionibacterium acnes pueden estar asociadas a las osteomielitis con osteosíntesis y, en estas situaciones, es importante alargar el tiempo de incubación de las placas de cultura por hasta 14 días permitiendo la identificación de patógenos que crecen lentamente en las culturas en medio sólido.(15) Desde luego, las culturas de tejido óseo pueden producir resultados falso negativos en hasta 40% de los casos, principalmente en los pacientes que ya están previamente en uso de antibióticos.(16) En los casos de osteomielitis con osteosíntesis o en las artroplastias infectadas, la técnica de sonicación de los implantes, retirados quirúrgicamente, aumentan de modo significativo la identificación de los patógenos (bacterias y levaduras) contenidos en los biofilmes que están Lima ALLM, et al. • Directrices panamericanas para el tratamiento de las osteomielitis... adheridos a los implantes y que son liberados para el tejido óseo causando osteomielitis. La sonicación consiste en someter los implantes quitados quirúrgicamente y de forma estéril, a la travesía de ultrason de baja frecuencia y consecuente ruptura de la superficie de protección polimérica extracelular que protege las bacterias contenidas en los biofilmes. Las bacterias liberadas de los biofilmes en medio líquido se mantienen factibles y son cultivadas en medios de cultura sólidos y líquidos.(17) En 79 pacientes con infecciones asociadas a prótesis articulares, la sensibilidad de las culturas producidas por medio de muestras de tejido óseo o por el fluido de sonicación de los implantes fue de 60.8% y 78.5% respectivamente (P<0.001) en trabajo publicado por Trampuz y cols., mientras que en otra muestra de pacientes con infecciones óseas asociadas a los implantes ortopédicos, la sensibilidad de las culturas de hueso y del líquido de sonicación fue de 61.1% y 83.3% (P=0.008), respectivamente. En los dos estudios, estas diferencias fueron aún más grandes cuando los pacientes estaban en uso de antibióticos en el momento de la recolección de las culturas.(18,19) Recomendaciones para recolección de muestras para diagnóstico(20-22) Hemoculturas: Las hemoculturas deben ser recolectadas en las osteomielitis agudas o posoperatório inmediato de las osteomielitis crónicas; La antisepsia de la piel deberá ser rigurosa, una vez que bacterias presentes en la microbiota cutánea, a ejemplo de S. epidermidis y Propionibacterium sp, son igualmente potenciales agentes etiológicos. Debe ser realizada con solución alcohólica de clorexidina. En adultos o niños con masa corpórea superior a 30 kg, recolectar dos muestras de 20 ml cada, de sitios distintos, e inocular cada muestra en un frasco para aerobios y un frasco para anaerobios, después de la asepsia de los septos con etanol a 70%, totalizando cuatro frascos con 10 ml cada; En niños con hasta 30 kg, recolectar una sola muestra de 5 ml o volumen proporcional a la masa corpórea e inocular en frasco para aerobios. En caso de sospecha de infección por anaerobio el mismo volumen de sangre debe ser inoculado en frasco específico. Muestras producidas por procedimientos invasivos: En las osteomielitis crónicas la terapia antimicrobiana debe ser interrumpida por lo menos 30 días antes del procedimiento de recolección para rifampicina, fl uorquinolonas y ciclinas; para los demás antimicrobianos el plazo mínimo debe ser de 15 días; No recolectar material originario de fístulas, pues las bacterias presentes en la muestra frecuentemente representan solo colonización del trayecto o microbiota cutánea, y no el agente etiológico real; La recolección de muestras en el intraoperatório debe preceder la infusión de antimicrobianos; No enviar para el laboratorio fragmentos óseos con dimensiones superiores a 0,5 x 0,5 x 0,5 cm. La mayoría absoluta de los laboratorios no tiene condiciones de fragmentar hueso. Enviar múltiples pequeños fragmentos; Durante procedimiento quirúrgico recolectar un mínimo de cinco y máximo de diez muestras, preferencialmente trocando de instrumental a cada local de recolección; Fragmentos óseos o de tejidos blandos deben ser acondicionados en frascos plásticos desechables estériles conteniendo soro fisiológico estéril en volumen mínimo como para mantener el fragmento hidratado; No poner fragmentos o líquidos en el tubo de medio de transporte del swab. Introducir exclusivamente el swab utilizado para la recolección de muestra clínica; Recolectar un fragmento con dimensiones máximas de 0,5 x 0,5 x 0,5 cm para cada tipo de cultura, o sea, 1 para la cultura de fungos, 1 para la cultura para micobacterias y 1 para cultura general. Los fragmentos para cultura para fungos y para micobacterias, de un mismo local, pueden ser acondicionados en el mismo frasco estéril; Para cultura de fragmento óseo para anaerobios, solicitar al laboratorio tubo conteniendo medio de tioglicolato con resazurina. Recolectar uno o más fragmentos de 0,5 x 0,5 x 0,5 cm; destapar el tubo y transferir el(los) fragmento(s). Tapar inmediatamente. No refrigerar. Mantener el tubo en posición vertical, en temperatura ambiente durante el transporte para el laboratorio. Alternativamente aspirar el contenido de absceso e inyectar en frasco de hemocultura para anaerobios luego de la asepsia del septo con etanol a 70%; Los líquidos deben ser acondicionados en frascos plásticos desechables estériles. El volumen mínimo para cada cultura y examen directo es de 0,1 ml y el volumen ideal es de 1,0 ml. Volúmenes mayores aumentan la sensibilidad para fungos y micobacterias; Caso haya sospecha de Brucella el líquido aspirado debe ser inoculado en frasco de hemocultura para aerobios y el laboratorio debe ser avisado para alargar el tiempo de incubación para 14 días; Se recomienda que la muestra para exámenes de 19 Rev Panam Infectol 2013;15(1 Supl 1):17-25. biología molecular sea recolectada en frasco individual, plástico, desechable; La recolección de muestras de manera adecuada y en medios de transporte permite que la siembra se haga en hasta 24 horas manteniendo la factibilidad de los patógenos en temperatura ambiente; Pocos sistemas de transporte permiten mantener la factibilidad de anaerobios; el laboratorio debe ser consultado cuanto a la adecuación del sistema para tal. Transporte Muestras destinadas al cultivo de microorganismos no pueden ser congeladas sin crioprotector. Tan solo muestras destinadas a diagnóstico por biología molecular pueden ser congeladas para evaluación futura o complementar; Muestras conservadas en formol NO son adecuadas para diagnóstico microbiológico. Hemoculturas Deben ser transportadas en temperatura ambiente por hasta 12 horas. No refrigerar o incubar en estufa antes de la entrada en el aparato automatizado. Cultura general, para fungos, micobacterias y testes moleculares Deben ser transportadas en temperatura ambiente por hasta 1 hora, o por 24 horas bajo refrigeración (2 a 8°C). Cultura para anaerobios En el caso de que haya sido recolectada en frascos de hemocultura para anaerobios, deben ser transportadas en temperatura ambiente por hasta 12 horas. No refrigerar o incubar en estufa antes de la entrada en el aparato automatizado; Muestras recolectadas en medio de tioglicolato deben ser transportadas en temperatura ambiente por hasta 12 horas. No refrigerar. Transportar en la posición vertical, ya que el medio es fluido y su aeración – el medio presenta coloración rosa - es deletérea para anaerobios. Procesamiento El procesamiento de las muestras debe ser realizado en cabina de seguranza biológica; 20 Teniendo en cuenta la detección óptima de infecciones polimicrobianas, las muestras para cultura general deben ser inoculadas en medio de tioglicolato, agar sangre de carnero a 5%, agar chocolate suplementado con PolyVitex® o similar, agar MacConkey (selectivo para bacilos Gram negativos no exigentes) y agar sangre de carnero a 5% con feniletanol (selectivo para Gram positivos); Las placas de agar sangre y agar chocolate deben ser incubadas en estufa de CO2 a 5% a 36 ± 1°C por hasta 7 días. Las culturas para anaerobios se deben mantener en incubación por hasta 14 días(15). Colonias con características similares, pero tamaños distintos deben ser procesadas para identificación y teste de sensibilidad apartados. Testes de sensibilidad(23,24) Los testes de sensibilidad deben ser realizados con culturas puras y recientes; La sensibilidad a los glicopeptídeos deberá ser realizada por microdilución no automatizada o gradiente en medio sólido (Etest® o MICE®), y no se acepta la utilización del método de la discodifusión. El punto de corte para sensibilidad para teicoplanina, en función de la aprobación para uso clínico en Europa, pero no en los Estados Unidos, se recomendaría ser aquel preconizado por el European Committee on Antimicrobial Susceptibility Testing (EUCAST), según lo cual son considerados sensibles S. aureus con CIM < 2 mg/l y Staphylococcus coagulase negativos con CIM < 4 mg/l; El punto de corte de sensibilidad para vancomicina para S. aureus preconizado por el Clinical and Laboratorial Standards Institute (CLSI) y por el EUCAST difieren de las recomendaciones de la Infectious Diseases Society of America. Hasta que más evidencias científicas se acumulen, se recomienda utilizar el punto de corte para sensibilidad de 1,0 mg/l;(25) La investigación de resistencia inductiva a la clindamicina deberá ser realizada y reportada rutinariamente en los géneros Staphylococcus y Streptococcus;(26) La sensibilidad para rifampicina deberá ser investigada y reportada rutinariamente para el género Staphylococcus. Lima ALLM, et al. • Directrices panamericanas para el tratamiento de las osteomielitis... Avances en el diagnóstico A) Microbiología El aislamiento en medio de cultura todavía es el método de elección para el diagnóstico de las osteomielitis, por permitir la realización de los testes de sensibilidad; sin embargo, los métodos moleculares representan una herramienta indispensable en la aclaración de la etiología de infecciones cuyo cultivo de las muestras clínicas resultan negativos, ya sea por uso previo de antimicrobianos o condiciones inadecuadas de cultura. La mayoría de las bacterias posee múltiples copias de genes que codifican el RNA ribosómico, con regiones hipervariables y regiones conservadas. La utilización de iniciadores que anillan en regiones conservadas, flanqueando regiones hipervariables, ha sido la principal estrategia para la detección de patógenos. Luego de la extracción del DNA, la muestra es utilizada para reacción de PCR y el producto amplificado es purificado y luego sometido a la reacción de secuenciación de DNA. Los productos de la reacción de secuenciación son separados y analizados en secuenciadores automáticos. La secuencia que se obtiene es comparada con aquellas disponibles en el GenBank.(27,28) Diferentemente de los procedimientos de cultura, que deben tener el transporte reducido al menor tiempo posible, las muestras para testes moleculares son estables por tiempo indeterminado si conservadas en temperatura igual o menor que -80°C. Las desventajas de los testes moleculares son el coste más elevado y la necesidad de técnicas de clonaje en caso de infección polimicrobiana. Algunos sistemas comerciales, a ejemplo de SeptiFast y PlexId son capaces de detectar e identificar infecciones polimicrobianas y mecanismos de resistencia, a ejemplo del gene mecA que codifica resistencia a la oxacilina en Staphylococcus; con todo, no fueron originalmente concebidos para uso en diagnóstico de osteomielitis.(29,30) B) Imagen Introducción El uso de métodos de imagen complementares puede ser importante en el diagnóstico precoz de las osteomielitis. Asimismo, puede auxiliar en el comienzo rápido y en el acompañamiento evolutivo de la respuesta al tratamiento, permitiendo cambios de los no efectivos. A pesar de no haber consenso sobre el mejor flujograma de exámenes de imagen a ser utilizado en la evaluación de las osteomielitis, clásicamente en literatura médica, encontramos publicaciones involucrando métodos de radiología convencional, resonancia magnética, tomografía computadorizada, ultrasonografía y métodos de medicina nuclear. Figura 1. Edema de la medula ósea (áreas mal definidas de hiposinal en las secuencias ponderadas en T1 e hipersinal en T2, con realce poscontraste) (Fuente: Dr. Marcelo Bordalo Rodrigues) Radiografía simple En las osteomielitis agudas, la radiografía simple (rayos X) no demuestra cualesquier alteraciones. Después de cerca de 3-4 días, puede haber un aumento de tejidos blandos. Las alteraciones óseas aparecen después de dos semanas, y pueden ser observadas lesiones líticas mal delimitadas, simulando una lesión agresiva. Lo mismo se puede observar una reacción periosteal lamelar. El rayo X presenta positividad de apenas 20% después de dos semanas, y es un método de baja sensibilidad, necesario, con todo, para excluir otras afecciones (tumores, fracturas). Nivel de evidencia: 3. Resonancia magnética La resonancia magnética (RM) está considerada la principal modalidad por imagen en la evaluación de las infecciones óseas, y se observan alteraciones precoces desde los primeros días de enfermedad. Se nota edema de la medula ósea (áreas mal definidas de hiposinal en las secuencias ponderadas en T1 e hipersinal en T2, con realce poscontraste) (figura 1). Con la progresión de la enfermedad, se puede observar el surgimiento de abscesos, con el típico realce periférico al contraste. Característicamente, la infección atraviesa el cartílago de crecimiento, al revés de las alteraciones neoplásicas. Asimismo se puede observar reacciones periosteales y edemas de tejidos blandos. La especificidad de la RM es mayor que la del centellograma óseo para el diagnóstico de infección. Nivel de evidencia: 2. Tomografía computadorizada La tomografía computadorizada (TC) tiene poca utilidad en el diagnóstico de la infección aguda. Su 21 Rev Panam Infectol 2013;15(1 Supl 1):17-25. papel se restringe tan solo para la investigación de secuestro óseo en el caso de infecciones subagudas y crónicas, indicando una potencial actividad de la infección. Nivel de evidencia: 5. Ultrasonografía El examen por ultrasonido puede tener su utilidad especialmente en los pacientes más jóvenes, demostrando edema de tejidos blandos yuxtaoseo, espesamientos periosteales y colecciones subperiosteales. Se observa un área de hiperemia al Doppler colorido. Este método ofrece pocos datos en relación a extensión interósea, y es de poca utilidad en esta indicación. Nivel de evidencia: 2. Seguimiento evolutivo del tratamiento Los métodos por imagen presentan poca utilidad en el acompañamiento terapéutico de las infecciones óseas. Las alteraciones radiológicas pueden permanecer presentes, a pesar del tratamiento satisfactorio. En esta situación, los métodos funcionales, especialmente el PET-CT, presentan un papel más importante. Nivel de evidencia: 2. Medicina nuclear La medicina nuclear echa mano de radiofármacos con propiedades biológicas conocidas, para de ahí trazar una imagen de un proceso fisiológico del organismo. A partir de alteraciones del metabolismo estudiado pueden ser establecidos los diagnósticos investigados. En los tópicos a seguir discutiremos más específicamente los posibles estudios de Medicina Nuclear y sus radiofármacos, poniendo de relieve sus particularidades y evidencias de literatura para su uso. Algunas de las indicaciones más comunes de los métodos de medicina nuclear son en la sospecha de osteomielitis con señales clínicos o radiográficos dudosos, cuando existen artefactos de imagen en los métodos radiológicos, y en el acompañamiento evolutivo o de respuesta al tratamiento instituido. Centellograma óseo El centellograma óseo es un examen históricamente utilizado para la diferenciación de osteomielitis de las infecciones de tejidos blandos. Utiliza como radiofármaco difosfonados marcados con tecnécio 99 metaestable (99mTc), siendo el metilenodifosfonato (99mTc -MDP) uno de los más comunes.(31) Es realizado en su modo denominado trifásico, siendo la primera fase de flujo con imágenes dinámicas adquiridas luego de la inyección endovenosa del radiofármaco, por 1 minuto; la segunda fase, de equilibrio, con imágenes estáticas de la región de más interés, se logra 5 minutos después de la inyección del radio- 22 fármaco, y la tercera fase, tardía, con imágenes de cuerpo entero, se alcanza después de 2 horas de la inyección del radiofármaco. Las imágenes de flujo y equilibrio demuestran respectivamente alteraciones de perfusión arterial e hiperemia presentes en procesos inflamatorios, mientras las imágenes tardías demuestran alteraciones del metabolismo osteogéno. La diferenciación entre celulitis y osteomielitis aparecen en las imágenes tardías ya que solo las osteomielitis presentan alteraciones del metabolismo óseo, mientras tanto las osteomielitis como las infecciones de tejidos blandos presentan hiperflujo sanguíneo e hiperemia en las fases de flujo y de equilibrio.(32) En general, las osteomielitis se presentan como áreas de hiperconcentración focal del radiofármaco en la fase tardía del centellograma óseo en el área sospechosa para las osteomielitis. A pesar de la satisfactoria sensibilidad (7089%), este estudio presenta baja especifi cidad (16-36%),(33,34) pues otros procesos como trauma y fracturas pueden llevar a remoldeamiento óseo, y porque en las primeras 24 horas pueden aun no tener pasado el comienzo do remoldeamiento óseo por la infección.(35) Puede, por lo tanto ser un método empleado después de 24 horas de inicio de la enfermedad y habitualmente es indicado como método inicial de medicina nuclear principalmente por su alto valor predictivo negativo, necesitando con todo ser complementado con métodos que presenten mayor especificidad cuando se presentar alterado. Puede demostrar focos insospechados por se tratar de un estudio de cuerpo entero, pero ocasionalmente estos focos pueden representar otras enfermedades.(35) Una forma de elevar la especificidad del método es el uso en la fase tardía de adquisiciones tomograficas por emisión de fotón único asociado a la tomografía computadorizada (SPECT-CT) de la área de interés,(36) pero esta tecnología todavía no es ampliamente disponible. Nivel de evidencia: 1. Centellograma con Galio-67 El citrato de galio-67 (67Ga) es un radiofármaco análogo al hierro que se concentra en sitios inflamatorios por mayor flujo sanguíneo y por aumento de la concentración de transferrina la cual es compleja. El centellograma es realizado con imágenes de cuerpo entero 24 y/o 48 horas después de la administración endovenosa del radiofármaco, y es utilizado para detección de focos infecciosos desconocidos.(37) Por ser un estudio de procesos inflamatorios es utilizado en la investigación de las osteomielitis como complementación al centellograma óseo con la finalidad de elevar la especificidad del diagnóstico. Lima ALLM, et al. • Directrices panamericanas para el tratamiento de las osteomielitis... Por el citrato de galio-67 se concentrar en procesos de remodelamiento óseo, los principales criterios interpretativos para determinar la osteomielitis cuando comparada al centellograma con galio-67 al centellograma óseo incluyen: mayor extensión y/o mayor intensidad del área de hiperconcentración del radiofármaco en el centellograma con galio, o ubicaciones diferentes de áreas de hiperconcentración de los radiofármacos cuando en los dos estudios (áreas discordes).(32) De nuevo la asociación del SPECT-CT puede elevar la exactitud diagnóstica, y puede ser asociado cuando disponible.(38,39) El uso de la asociación del centellograma con galio-67 es un método descrito y utilizado por su mayor disponibilidad, pero tiene limitaciones interpretativas y de exactitud, y no debe ser utilizado para diagnóstico cuando otras metodologías como el centellograma con leucocitos marcados o el PET-CT con FDG estuvieren disponibles. Algunos autores abogan su uso para acompañamiento terapéutico después de la antibioticoterapia o cirugía.(31) Nivel de evidencia: 3. Centellograma con leucocitos marcados El centellograma con leucocitos marcados con índio-111 (111In) o 99mTc-HMPAO, es una metodología de medicina nuclear muy estudiada en literatura médica. Está considerada la mejor metodología de medicina nuclear convencional, ya que refleja directamente el proceso de reclutamiento celular inflamatorio, y es totalmente independiente del remoldeamiento óseo, pero debemos acordarnos que presenta limitaciones cuando el foco es sospechoso en el esqueleto axial, con destaque para la columna vertebral.(31) Por ejemplo, la sensibilidad y especificidad para osteomielitis crónica es de respectivamente 84% y 80% en el esqueleto apendicular, mientras que es de respectivamente 21% y 60% en el esqueleto axial.(33) El proceso de marcación de los leucocitos es complexo e involucra extracción de muestra sanguínea del paciente, manipulación estéril de sangre para radiomarcación, y reinyección de los leucocitos marcados en el paciente, hechos que dificultan la difusión del método. Las imágenes de cuerpo entero son adquiridas 4 y 24 horas luego de la reinyección de los leucocitos marcados. En la evaluación de las osteomielitis crónicas presenta sensibilidad de 43-76% y especificidad de 63-87%, y cuando asociada interpretativamente al centellograma óseo presenta sensibilidad de 72-83% y especificidad de 75-90%.(33) Su confiabilidad es satisfactoria, y no es afectada por la influencia de antibioticoterapia; así que está considerado un estudio adecuado para acompañamiento posterapéutico.(40) Nivel de evidencia: 1. PET-CT con FDG La tomografía por emisión de positrones acoplada a la tomografía computadorizada (PET-CT) es un estudio que emplea isótopos emisores de positrón para formación de imágenes. Comparado al centellograma convencional se destaca por ser un método de imágenes seccionales con mayor resolución espacial. Puede utilizar diferentes radiofármacos como en los centellogramas, sin embargo, tiene como radiofármaco más disponible y ampliamente utilizado la fluordeoxiglicose marcada con flúor-18 (18F-FDG). La FDG es un radiofármaco marcador de metabolismo glicolítico, habitualmente elevado en procesos inflamatorios agudos y crónicos, y por lo tanto, propuesto como herramienta diagnóstica en estas situaciones, y presentando superioridad en exactitud diagnóstica cuando comparado a los demás métodos de medicina nuclear.(41) En meta-análisis evaluando osteomielitis sospechosa, la exactitud del PET-CT con FDG fue de 96,6% mientras el método convencional más cercano fue el centellograma con leucocitos marcados presentando 91,3%.(41) Ya en la evaluación de las osteomielitis crónicas, y en metaanálisis, fue el método de mayor exactitud, presentando sensibilidad y especificidad del 96% y 91% respectivamente, y son estos valores mayores que los logrados para centellograma óseo, centellograma con leucocitos marcados, centellograma óseo asociado al centellograma con leucocitos marcados, resonancia magnética y radiografía simple.(33) Sus resultados han sido evaluados como promisores en diversas áreas además de las osteomielitis crónicas(33) y de infección vertebral,(42,43) lo mismo de infecciones de prótesis ortopédicas.(43) Otra situación donde el PET-CT parece presentar ventajas sobre los métodos convencionales como resonancia magnética es el seguimiento de niños luego de las osteomielitis agudas, pues diferencia mejor infección de actividad de tejido reparadora/cicatricial. (44) Se espera que cada vez más sea confirmado en literatura médica el valor del PET-CT en la monitorización de respuesta terapéutica.(45) Con todo, a pesar de poder ser considerada una de las técnicas con mejores resultados, y con evidencias sólidas en literatura de su valor, hay situaciones clínicas donde el PET-CT puede presentar limitaciones. Estas limitaciones o dificultades interpretativas deben ser consideradas en el momento de solicitación de un examen de imagen para complementación diagnóstica.(46) Debemos acordarnos que entre sus limitaciones más importantes se incluyen el alto coste del examen y la pequeña disponibilidad del PET-CT cuando comparada al centellograma y métodos de radiología convencionales.(43) Nivel de evidencia: 1. 23 Rev Panam Infectol 2013;15(1 Supl 1):17-25. Otros radiofármacos Podemos citar otros radiofármacos que han sido utilizados a la manera de investigaciones en la literatura médica. Entre las más, evidenciamos para centellograma la biotina marcada con 111In, con destaque para las evaluaciones de columna vertebral donde los leucocitos marcados presentan harto conocida limitación.(47,48) Otro con reciente interés en literatura para centellograma son los antibióticos radiomarcados donde se destaca la ciprofloxacina marcada con 99mTc (49,50) que se está investigando en las infecciones óseas. Para PET-CT algunos radiofármacos que se están estudiando son el fluoreto de sodio marcado con 18F y el citrato de Galio 68 (68Ga), los cuales serían los equivalentes del centellograma óseo y del centellograma con Galio para se realizar PET-CT óseo y PET-CT con Galio, respectivamente. (51,52) Todos estos radiofármacos son de investigación y de momento todavía no pueden tener su uso recomendado en la rutina clínica. Nivel de evidencia: 5. Referencias 1. Calhoun JH, Manring MM. Adult Osteomyelitis. Infect Dis Clin North Am 2005;19(4):765-86. 2. Lew DP, Waldvogel FA. Osteomyelitis. Lancet 2004; 364(9431):369-79. 3. Dinh MT, Abad CL, Safdar N. Diagnostic accuracy of the physical examination and imaging tests for osteomyelitis underlying diabetic foot ulcers: meta-analysis. Clin Infect Dis 2008;47(4):519-27. 4. Unkila-Kallio L, Kallio MJ, Eskola J, Peltola H. Serum C-reactive protein, erythrocyte sedimentation rate, and white blood cell count in acute hematogenous osteomyelitis of children. Pediatrics 1994;93(1):59-62. 5. Roine I, Faingezicht I, Arguedas A, Herrera JF, Rodríguez F. Serial serum C-reactive protein to monitor recovery from acute hematogenous osteomyelitis in children. Pediatr Infect Dis J 1995;14(1):40-4. 6. Mutluoglu M, Uzun G, Ipcioglu OM, Sildiroglu O, Özcan Ö, Turhan V, Mutlu H,Yildiz S. Can procalcitonin predict bone infection in people with diabetes withinfected foot ulcers? A pilot study. Diabetes Res Clin Pract 2011;94(1):53-6. 7. Faesch S, Cojocaru B, Hennequin C, Pannier S, Glorion C, Lacour B, Chéron G. Can procalcitonin measurement help the diagnosis of osteomyelitis and septic arthritis? A prospective trial. Ital J Pediatr 2009;35(1):33. 8. Butbul-Aviel Y, Koren A, Halevy R, Sakran W. Procalcitonin as a diagnostic aid in osteomyelitis and septic arthritis. Pediatr Emerg Care 2005;21(12):828-32. 9. Berbari E, Mabry T, Tsaras G, Spangehl M, Erwin PJ, Murad MH, Steckelberg J,Osmon D. Inflammatory blood laboratory levels as markers of prosthetic joint infection: a systematic review and meta-analysis. J Bone Joint Surg Am 2010;92(11):2102-9. 10. Ochsner PE, Hailemariam S. Histology of osteosynthesis associated bone infection. Int. J. Care Injury 2006;37 Suppl 2:S49-58. 11. Zuluaga AF, Galvis W, Saldarriaga JG, Agudelo M, Salazar BE, Vesga O. Etiologic diagnosis of chronic osteomyelitis: a prospective study. Arch Intern Med 2006;166(1):95-100. 24 12. Wu JS, Gorbachova T, Morrison WB, Haims AH. Imaging guided bone biopsy for osteomyelitis: are there factors associated with positive or negative cultures? AJR Am J Roentgenol 2007;188:1529-34. 13. Tohtz SW, Müller M, Morawietz L, Winkler T, Perka C. Clin Orthop Relat Res 2010;468(3):762-8. 14. Senneville E, Morant H, Descamps D, et al. Needle puncture and transcutaneous bone biopsy cultures are inconsistent in patients with diabetes and suspected osteomyelitis of the foot. Clin Infect Dis 2009;48(7):888-93. 15. Schäfer P, Fink B, Sandow D, Margull A, Berger I, Frommelt L. Prolonged bacterial culture to identify late periprosthetic joint infection: a promising strategy. Clin Infect Dis 2008;47(11):1403-9. 16. Cataldo MA, Petrosillo N, Cipriani M, Cauda R, Tacconelli E. Prosthetic joint infection: recent developments in diagnosis and management. J Infect 2010;61(6):443-8. 17. Pitt WG, Ross SA. Ultrasound increases the rate of bacterial cell growth. Biotechnol Prog 2003;19(3):1038-44. 18. Trampuz A, Piper KE, Jacobson MJ, Hanssen AD, Unni KK, Osmon DR, Mandrekar JN, Cockerill FR, Steckelberg JM, Greenleaf JF, Patel R. Sonication of removed hip and knee prostheses for diagnosis of infection. N Engl J Med 2007;357(7):654-63. 19. Holinka J, Bauer L, Hirschl AM, Graninger W, Windhager R, Presterl E. Sonication cultures of explanted components as an add-on test to routinely conducted microbiological diagnostics improve pathogen detection. J Orthop Res 2011;29(4):617-22. 20. Corvec S, Loiez C, Portillo ME, Rottmann M & Trampuz A. Bone and Joint Infections. in European manual of Clinical Microbiology (Eds. Cornaglia, G., et al.) 469. European Society for Clinical Microbiology and Infectious Diseases, France 2012. 21. Baron EJ, Thomson RBJ. Specimen Collection, Transport and Processing: Bacteriology. in Manual of Clinical Microbiology;1 (Ed. Versalovic, J.):1261. American Society for Microbiology, United States 2012. 22. Carlsson J, Sundqvist G. Evaluation of methods of transport and cultivation of bacterial specimens from infected dental root canals. Oral Surg Oral Med Oral Pathol 1980;49(5):451-4. 23. Clinical and Laboratory Standards Institute (CLSI). Performance Standards for Antimicrobial Susceptibility Testing - TwentySecond Informational Supplement - M100-S22 Document. (CLSI, Wayne, Pensylvania - USA 2012). Data form: www. clsi.org. 24. European Committee on Antimicrobial Susceptibility Testing. Data from the EUCAST MIC distribution website, last accessed Oct 2012. http://www.eucast.org. 25. Rybak, M.J., et al. Vancomycin therapeutic guidelines: a summary of consensus recommendations from the infectious diseases Society of America, the American Society of HealthSystem Pharmacists, and the Society of Infectious Diseases Pharmacists. Clinical infectious diseases: an official publication of the Infectious Diseases Society of America 2009;49:325-7. 26. Lewis JS 2nd, Jorgensen JH. Inducible clindamycin resistance in Staphylococci: should clinicians and microbiologists be concerned? Clin Infect Dis 2005;40(2):280-5. 27. Rampini SK, Bloemberg GV, Keller PM, Büchler AC, Dollenmaier G, Speck RF, Böttger EC. Clin Infect Dis 2011;53(12):1245-51. 28. Clinical and Laboratory Standards Institute (CLSI). Interpretative Criteria for Identification of Bacteria and Fungi by DNA Target Sequencing; CLSI Document MM18-A. (Clinical and Laboratory Standards Institute, Wayne, Pensylvania - USA). 2008. Data form: www.clsi.org. 29. Harris LG, El-Bouri K, Johnston S, Rees E, Frommelt L, Siemssen N, Christner M, Davies AP, Rohde H, Mack D. Rapid Lima ALLM, et al. • Directrices panamericanas para el tratamiento de las osteomielitis... 30. 31. 32. 33. 34. 35. 36. 37. 38. 39. 40. 41. identification of staphylococci from prosthetic joint infections using MALDI-TOF mass-spectrometry. Int J Artif Organs 2010;33(9):568-74. Mencacci A, Leli C, Cardaccia A, Montagna P, Moretti A, Bietolini C, Meucci M, Perito S, Cenci E, Bistoni F. Comparison of conventional culture with SeptiFast real-time PCR for microbial pathogen detection in clinical specimens other than blood. JJ Med Microbiol 2011;60(Pt 12):1774-8. Concia E, Prandini N, Massari L, Ghisellini F, Consoli V, Menichetti F, Lazzeri E. Osteomyelitis: clinical update for pratical guidelines. Nucl Med Commun 2006;27:645-60. Sandler MP, Coleman RE, Patton JA, Wackers FJT, Gottschalk A. Diagnostic Nuclear Medicine, 4th ed., Lippincott Williams & Wilkins 2003. Termaat MF, Raijmakers PG, Scholten HJ, Bakker FC, Patka P, Haarman HJ. The accuracy of diagnostic imaging for the assessment of chronic osteomyelitis: a systematic review and meta-analysis. J Bone Joint Surg Am 2005;87(11):2464-71. Dinh MT, Abad CL, Safdar N. Diagnostic accuracy of the physical examination and imaging tests for osteomyelitis underlying diabetic foot ulcers: meta-analysis. Clin Infect Dis 2008;47(4):519-27. Dormans JP, Drummond DS. Pediatric hematogenous osteomyelitis: new trends in presentation, diagnosis and treatment. J Am Acad Orthop Surg 1994;2:333-41. Abdullah ZS, Khan MU, Kodali SK, Javaid A. Pyomiositis mimicking osteomyelitis detected by SPECT/CT. Hell J Nucl Med 2010;13(3):277-79. Chen WC, Tsai KD, Chen CH, Lin MS, Chen CM, Shih CM, Chen W. Role of gallium 67 scintigraphy in the evaluation of occult sepsis in the medical ICU. Intern Emerg Med 2012;7(1):53-8. Bar-Schalom R, Yefremov N, Guralnik L, Keidar Z, Engel A, Nitecki S, Israel O. SPECT/CT using 67Ga and 111In labeled leukocyte scintigraphy for diagnosis of infection. J Nucl Med 2006;47(4):587-94. Schillaci O. Hybrid imaging systems in the diagnosis of osteomyelitis and prosthetic joint infection. Q J Nucl Med Mol Imaging 2009;53(1):95-104. Liberatore M, Calandri E, Pavoni GL, Baiocchi P, Iurilli AP, Venditti M, Al-Nahhas A, Rubello D. Reliability of White blood cell scan in the follow-up of osteomyelitis. Biomed Pharmacother 2007;61(5):272-76. Wang G, Zhao K, Liu Z, Dong M, Yang S. A meta-analysis of 42. 43. 44. 45. 46. 47. 48. 49. 50. 51. 52. fluorodeoxyglucose-positron emission tomography versus scintigraphy in the evaluation of suspected osteomyelitis. Nucl Med Commun 2011;32:1134-42. Kim SJ, Kim IJ, Suh KT, Kim YK, Lee JS. Prediction of residual disease of spine infection using F-18 FDG PET/CT. Spine 2209;34(22):2424-30. Strobel K, Stumpe D. PET/CT in musculoskeletal infection. Semin Musculoskelet Radiol 2007;11(4):353-64. Warmann SW, Dittmann H, Seitz G Bares R, Fuchs J, Schaffer JF. Follow-up of acute osteomyelitis in children: the possible role of PET/CT in selected cases. J Pediatr Surg 2011;46(8):1550-56. Kumar R, Basu S, Torigian D, Anand V, Zhuang H, Alavi A. Role of modern imaging techniques for diagnosis of infection in the era of 18F-fluorodeoxyglucose pósitron emission tomography. Clin Microbiol Rev 2008;21(1):209-24. Liu Y. Orthopedic surgery-related benign uptake on FDG-PET: case examples and pitfalls. Ann Nucl Med 2009;23(8):701-8. Lazzeri E, Erba P, Perri M, Tascini C, Doria R, Giorgetti J, Mariani G. Scintigraphic imaging of vertebral osteomyelitis with 111In-biotin. Spine 2008;33(7):E298-204. Lazzeri E, Erba P, Perri M, Doria R, Tascini C, Mariani G. Clinical impacto f SPECT/CT with In-111 biotin on the managment of patients with suspected spine infection. Clin Nucl Med 2010;35(1):12-17. Singh B, Sunil HV, Sharma S, Prasad V, Kashyap R, Bhattacharya A, Mittal Br, Taneja A, Rai R, Goni VG, Aggarwal S, Gill SS, Bhatnagar A, Singh AK. Efficacy of indigenously developed single vial kit preparation of 99mTc-ciprofloxacin in the detection of bacterial infection: an Indian experience. Nucl Med Commun 2008;29(2):1123-29. Fuster D, Soriano A, Garcia S, Piera C, Suades J, Rodríguez D, Martinez JC, Mensa J, Campos F, Pons F. Usefulness of 99mTcciprofloxacin scintigraphy in the diagnosis of prosthetic joint infections. Nucl Med Commun 2011;32(1):44-51. Gemmel F, Van der Wyngaert H, Love C, Welling MM, Gemmel P, Palestro CJ. Prosthetic joint infections: radionuclide stateof-the-art imaging. Eur J Nucl Med Mol Imaging 2012, [Epub ahead of print]. Nanni C, Errani C, Boriani L, Fantini L, Ambrosini V, Boschi S, Rubello D, Pettinato C, Mercuri M, Gasbarrini A, Fanti S. 68 Ga-citrate PET/CT for evaluating patients with infectious of the bone: preliminary results. J Nucl Med 2010;51(12):1932-36. 25